
禮來口服減肥藥頭對頭戰勝口服司美格魯肽。
9月18日,界面新聞記者從禮來獲悉,禮來口服GLP-1藥物orforglipron在2型糖尿病血糖控制和減肥頭對頭試驗中優于諾和諾德的口服司美格魯肽。
Orforglipron是一種在研、每日一次的小分子(非肽類)口服GLP-1受體激動劑,可在全天任何時間服用,無需飲食或飲水方面的限制。不過,Orforglipron尚未在中國獲批。
界面新聞了解,orforglipron在2型糖尿病成人患者的血糖控制效果方面優于口服司美格魯肽。
在主要終點上,orforglipron最高劑量組糖化血紅蛋白(A1C)降幅為2.2%,而口服司美格魯肽最高劑量組糖化血紅蛋白降幅為1.4%。
此外,在一項次要終點上,37.1%接受最高劑量orforglipron的參與者實現了糖化血紅蛋白 <5.7%,而在接受口服司美格魯肽最高劑量的參與者中這一比例僅為12.5%。
身體里的紅細胞含有血紅蛋白,它會和血糖發生結合。當血糖水平長期偏高時,被糖化的血紅蛋白比例就會升高。檢查時測的糖化血紅蛋白就是紅細胞里被糖基化的比例。
這意味著,orforglipron不僅比口服司美格魯肽降糖效果更好。此外,控糖深度也更為顯著。在orforglipron組里,有三成患者的血糖接近健康人的水平。在口服司美格魯肽組,只有1成患者左右能做到。
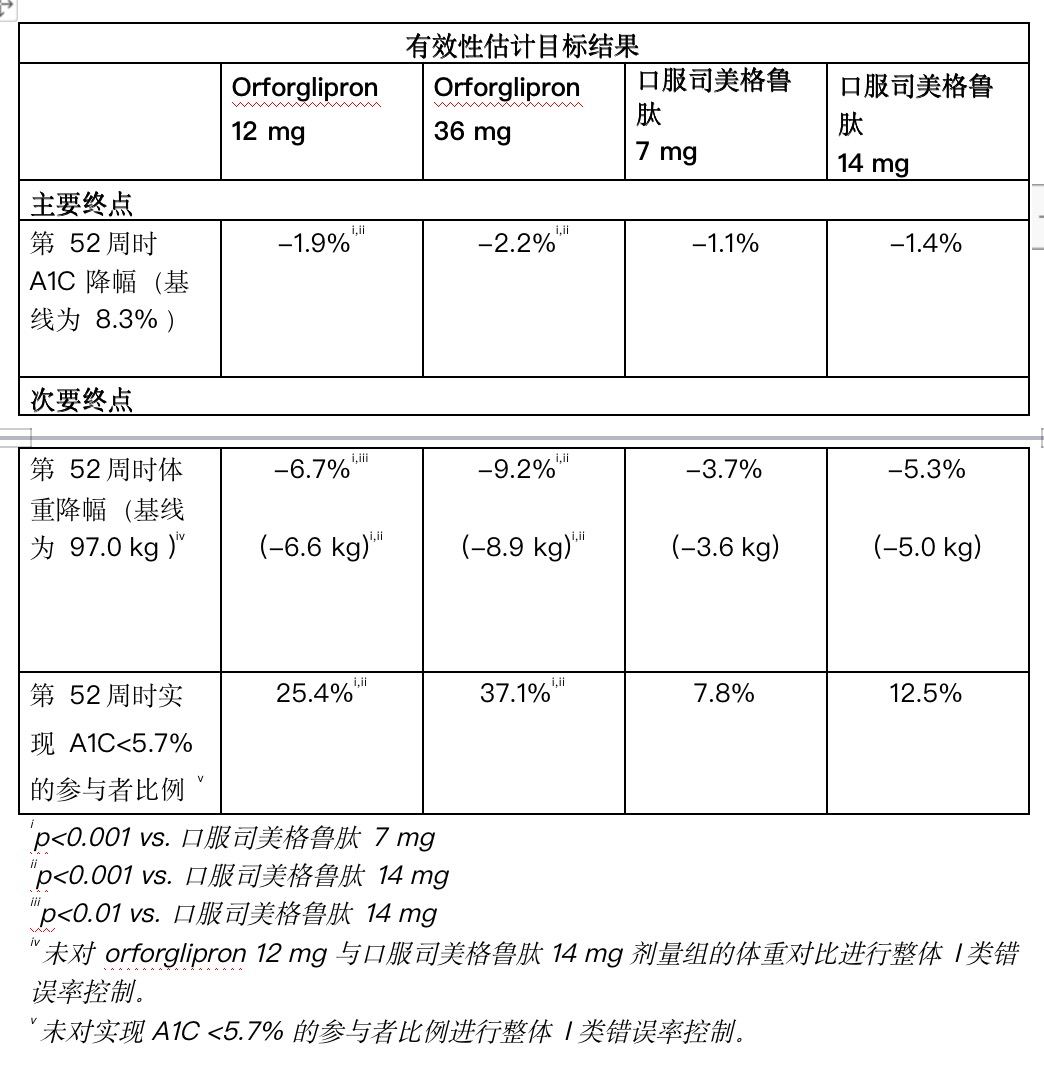
在關鍵次要終點方面,平均減重8.9 kg(9.2%),而口服司美格魯肽平均減重5.0 kg(5.3%),orforglipron的降幅提升73.6%。
Orforglipron的安全性和耐受性與以往研究結果一致。最常見的不良事件為胃腸道相關反應,通常為輕至中度。
該研究結果基于一項開放標簽、隨機的3期臨床研究。該研究在1698名經二甲雙胍治療血糖控制不佳的2型糖尿病成人參與者中,評估了orforglipron對比口服司美格魯肽的安全性和有效性。
禮來和諾和諾德的GLP-1藥物迭代戰役已經打響。競爭方向主要集中在三方面:注射制劑的長效化升級、給藥方式的口服化以及作用機制的多靶點拓展。
兼具較高患者依從性和用藥便捷性的口服制劑是當前雙方對抗最核心的戰場。截至目前,全球尚無口服GLP-1藥物獲批體重管理適應癥,能率先拿下“首個”頭銜,可能決定未來三年的競爭格局。
在口服GLP-1領域,諾和諾德起步最早。這使得諾和諾德在全球口服GLP-1藥物賽道贏得先機。
2019年,諾和諾德研發的全球首個口服GLP- 1藥物Rybelsus(治療成人2型糖尿病)獲得美國食品藥品監督管理局(FDA)批準上市。2024年1月,降糖版司美格魯肽口服制劑(商品名:諾和忻)也在中國獲批上市。
但在減重適應癥方面,諾和諾德的進展卻相對緩慢。2023年,諾和諾德公布了口服版減重司美格魯肽的Ⅲ期臨床試驗結果,但因產能受限,選擇推遲提交上市申請。
這一遲滯為禮來提供了追趕機會。其口服GLP-1藥物在開發戰略上甚至優先布局減重適應癥。
今年4月17日,禮來公布了其口服小分子GLP-1藥物orforglipron的研究結果,并表示預計將在今年年底前向全球監管機構提交Orforglipron用于體重管理的上市申請。
面對禮來的加速追擊,諾和諾德也不能再拖沓。于是,在禮來宣布消息不久,諾和諾德馬上將口服減重版司美格魯肽的上市申請提上日程。
進度上,諾和諾德還是領先。4月21日,諾和諾德宣布,公司已向美國食品藥品監督管理局提交口服Wegovy減重適應癥的上市申請。5月2日,諾和諾德再披露,美國食品藥品監督管理局已受理為該藥上市申請,預計將在2025年第四季度完成審評。
而據禮來介紹,其預計將在今年年底前向全球監管機構提交Orforglipron用于體重管理的上市申請,預計于2026年提交其用于治療2型糖尿病的上市申請。
 還未登錄
還未登錄
![]()